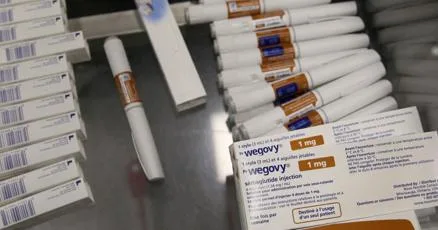
美國可能因 Hims 短暫推出 Wegovy 複方版而開罰
Hims & Hers 短暫推出 Novo Nordisk 的 Wegovy 49 美元複方版,引發 FDA 迅速反擊並轉介 DOJ。專家表示,美國可能因違反藥物法而開罰或禁制令,儘管 Hims 迅速撤回可能限制行動。這突顯複方 GLP-1 與核准減重藥之間的緊張,在需求激增中。
本页内容
美國可能因 Hims 短暫推出 Wegovy 複方版而開罰
在 GLP-1 藥物如 Wegovy 快速演變的世界中,線上遠距醫療提供商 Hims & Hers 最近的爭議突顯了對複方版本的監管審查。特朗普政府可能對 Hims 採取行動,包括禁制令或罰款,因為其有意銷售 Novo Nordisk 的 Wegovy 減重藥複方版,不過法律選項可能因 Hims 迅速撤回而受限,律師和其他專家告訴路透社。
事件經過:Hims 短暫 Wegovy 仿製品推出
Hims and Hers Health 上週宣布將提供 Novo Nordisk 的 Wegovy 減重藥更便宜的 49 美元版本,這是一種基於司美格魯肽的 GLP-1 促效劑,已獲准用於慢性體重管理。此舉發生在暢銷減重藥需求暴增之際,但 Hims 在食品藥物管理局 (FDA) 警告將對公司採取行動後迅速退讓。
FDA 隨後將 Hims 轉介給司法部 (DOJ) 以調查潛在法律違規,根據美國衛生與公眾服務部 (HHS) 總法律顧問 Mike Stuart 的說法。此轉介突顯政府執法藥物核准標準的決心,特別是針對如 Wegovy 和 Eli Lilly 競爭產品等高需求 GLP-1 藥物。
Wegovy 與 GLP-1 需求背景
Wegovy(司美格魯肽注射劑)透過模擬 GLP-1 激素來調節血糖、延緩胃排空並減少食慾,在臨床試驗中帶來顯著減重效果。Novo Nordisk 和競爭對手 Eli Lilly 努力滿足產品需求激增,儘管增加生產但供應短缺持續。這刺激了對複方替代品的興趣,這些替代品將司美格魯肽等活性成分與客製賦形劑混合。
然而,減重藥製造商主張某些複方藥商非法行銷未核准仿製品,規避 FDA 的嚴格安全與療效測試。
對 Hims 的潛在法律行動
司法部可能尋求法院禁制令或民事或刑事罰款,對 Hims 違反《聯邦食品、藥品及化妝品法》(FD&C Act)行銷未核准藥物,三位接受路透社訪談的律師表示。
「當你比較複方藥商與製藥產業整體,這些複方藥商並未花費巨資確保安全與療效,」HHS 總法律顧問 Mike Stuart 周一告訴 CNBC。
回應下一步問題時,HHS 指向 Stuart 先前聲明,強調保護製藥業對 FDA 核准途徑的投資。
Hims 未回應這些發展的置評要求。
複方藥物:何時合法?
根據《聯邦食品、藥品及化妝品法》(FD&C Act)的狹窄條款,美國複方藥物在藥物短缺或因醫療需求而患者特定客製化時合法。若無這些條件,FDA 可對規避商業可用產品核准的複方藥商執法,三位律師告訴路透社。
Hims 主張其產品合法,因為它們依患者醫療需求客製化。然而,Hims 的 Wegovy 複方版是否「足夠個人化」仍不明朗,因為其製造與處方實務的公開細節有限,两位 FDA 法規專家表示。
執法途徑:FDA、DOJ 與檢查
作為下一步,FDA 可能檢查 Hims 記錄以驗證處方文件是否適當,可能與授權複方藥房的州監管機構合作,Foley & Lardner 合夥人 Nathan Beaver 表示。
为您的治疗精准把关
加入数千使用Shotlee来精确追踪GLP-1药品进度及其副作用的人吧。
📱 免费使用 Shotlee
加入数千使用Shotlee来精确追踪GLP-1药品进度及其副作用的人吧。
由於 Hims 周六宣布不再提供複方減重藥,DOJ 可能選擇不繼續。「如果 Hims 已退讓並表示我們不做了,這裡並不明顯有案件或爭議,」Epstein, Becker & Green, P.C. 律師 James Boiani 表示。
政府可能將焦點轉移至 Hims 其他基於司美格魯肽的複方注射減重藥。這些情況更複雜,因為不同劑量與非活性成分讓複方藥商能更具說服力地主張合法性,Lowenstein Sandler 的 FDA 法規實務主席 James Shehan 表示,他曾任 Novo Nordisk 總法律顧問。
FDA-DOJ 合作
FDA 缺乏獨立訴訟權力,依賴 DOJ 執法。兩機構密切合作:FDA 法律顧問解釋《聯邦食品、藥品及化妝品法》,DOJ 主導訴訟。「如果 FDA 轉介,司法部通常會行動,」Shehan 表示。
這延續先前行動,如去年 9 月 HHS 對 Novo、Hims 等發出誤導廣告警告函。2 月 5 日,FDA 告知 Novo 其 Wegovy 電視廣告誤導性地暗示優於其他 GLP-1 藥物。
對 GLP-1 藥物與複方製程的影響
此事件突顯 GLP-1 市場的更廣緊張關係。經核准藥物如 Wegovy 經歷廣泛試驗證明安全與療效,包括心血管益處與長期資料。複方司美格魯肽缺乏此審查,增加劑量不一致、污染或不良反應風險。
使用複方 GLP-1 的患者應監測副作用如噁心、腸胃問題或罕見胰臟炎—這類藥物常見。Shotlee 等工具可幫助追蹤症狀與用藥時程,以利與醫師討論。
品牌藥 vs. 複方藥:關鍵差異
- 品牌藥 (Wegovy): FDA 核准、固定劑量 (0.25mg 至 2.4mg 每週)、證明穩定性與純度。
- 複方藥: 客製劑量/成分,僅在短缺或個人化時合法;無 FDA 上市前審查。
隨著某些 GLP-1 短缺緩解,FDA 對複方藥商的執法加劇,優先患者安全。
患者應知複方 GLP-1 的重點
若考慮司美格魯肽用於減重或糖尿病,優先 FDA 核准選項。與醫師討論複方需求—僅在品牌藥不可用且需個人化時追求。
諮詢遠距醫療處方提供者,驗證藥房執照。向 FDA MedWatch 報告不良事件。
安全考量
如 Wegovy 的 GLP-1 藥物帶有黑框警告,警示甲狀腺腫瘤 (囓齒動物資料) 與胃輕癱等風險。複方版本無標準品質控制,放大不確定性。
重點摘要
- Hims 49 美元 Wegovy 複方計劃引發 FDA 轉介 DOJ,可能依《聯邦食品、藥品及化妝品法》罰款/禁制令。
- 迅速撤回可能避免行動,但對其他司美格魯肽注射劑的審查持續。
- 複方僅在短缺/個人化時合法;專家質疑 Hims 合規性。
- 保護製藥研發投資;優先安全有效的 GLP-1 取得。
- 患者:堅持核准藥物、追蹤健康、諮詢醫師。
結論:駕馭 GLP-1 法規
Hims-Wegovy 事件預示對複方 GLP-1 的更嚴格監督,平衡取得與安全。隨著需求成長,關注 FDA 更新並優先核准療法以達最佳成果。有關 GLP-1 副作用或替代方案等主題,請探索我們的司美格魯肽療法與代謝健康指南。
原文出处信息
原文由以下机构发表: Post and Courier.阅读原文 →