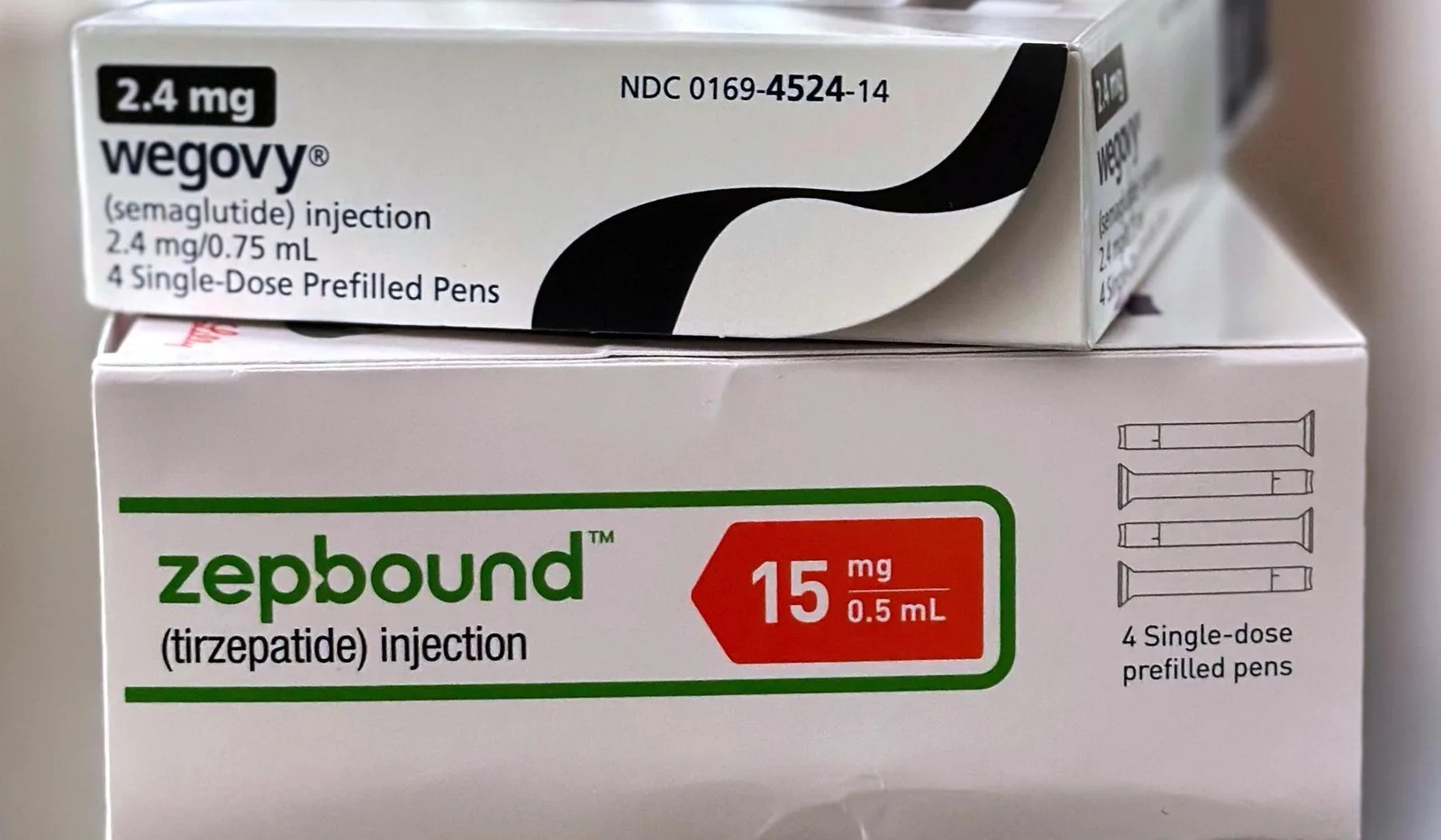
美國FDA要求移除GLP-1減重藥的自殺警示標籤
美國食品藥物管理局週二宣布,希望從GLP-1減重藥物移除自殺警示標籤。一項對91項試驗的全面審查顯示,使用者與安慰劑組相比,沒有更高的自殺念頭或行為風險。此變更使標籤與相同製造商的糖尿病藥物一致。
FDA的標籤變更提案
週二,美國食品藥物管理局宣布有意從GLP-1減重藥物中移除自殺警示標籤。
全面試驗結果
美國FDA檢視了91項試驗,將GLP-1使用者與安慰劑參與者進行比較。研究人員發現,60,338名使用減重藥物的人,並未顯示出比47,572名對照組更高的自殺念頭或行為風險。
本次更新的標的藥物
受影響的藥物包括Novo Nordisk以Saxenda品牌銷售的利拉魯肽;Novo Nordisk以Wegovy品牌銷售的司美格魯肽;以及Eli Lilly以Zepbound品牌銷售的替爾帕肽,依據美國FDA資料。
與糖尿病藥物一致
這些減重療法的擬議新標籤,將與其糖尿病適應症對應藥物一致—具體而言,即Novo Nordisk的Ozempic和Rybelsus,以及Eli Lilly的Mounjaro。
为您的治疗精准把关
加入数千使用Shotlee来精确追踪GLP-1药品进度及其副作用的人吧。
📱 免费使用 Shotlee
加入数千使用Shotlee来精确追踪GLP-1药品进度及其副作用的人吧。
這些糖尿病藥物在其標籤中,從未包含有關自殺念頭或行為的相關描述。
製造商聲明
Eli Lilly代表向Pharmaceutical Technology表示:「我們感謝美國FDA對此重要安全議題的謹慎考量。患者安全是Lilly的首要優先事項,我們將繼續與美國FDA合作,確保提供適當的安全資訊給處方醫師。」
Novo Nordisk發言人向Pharmaceutical Technology表示:「我們很高興看到美國FDA建議移除有關自殺意念及行為風險的警示……我們優先考量患者安全,並將繼續與美國FDA及其他監管機構密切合作。」
原文出处信息
原文由以下机构发表: Washington Times.阅读原文 →