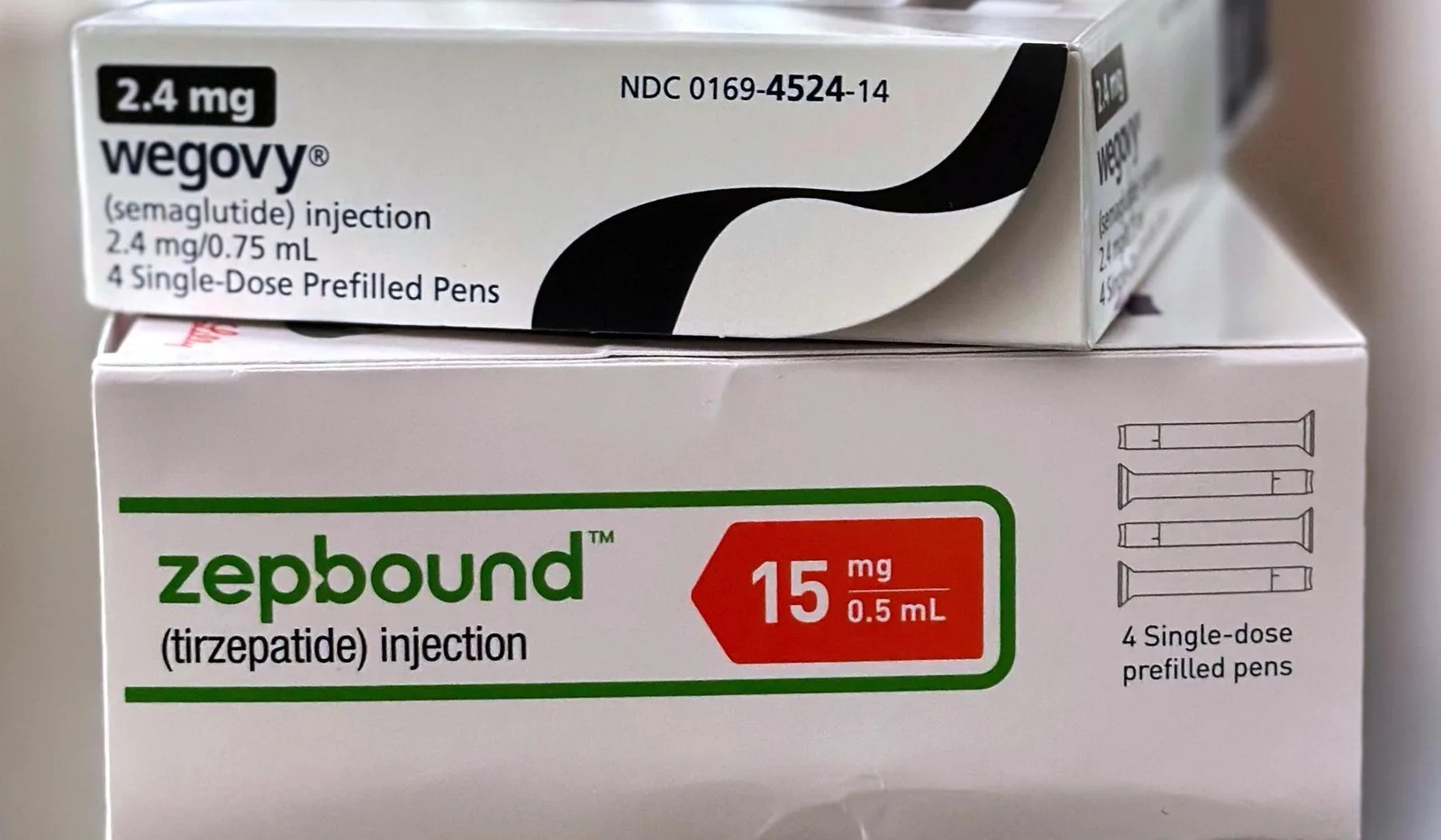
FDA solicita remoção de alertas de suicídio em medicamentos GLP-1 para emagrecimento
A Food and Drug Administration anunciou na terça-feira seu desejo de remover os rótulos de alerta de suicídio dos medicamentos para emagrecimento GLP-1. Uma revisão abrangente de 91 ensaios clínicos não revelou risco aumentado de pensamentos ou comportamentos suicidas entre usuários em comparação com grupos placebo. Essa mudança alinha os rótulos com os equivalentes para diabetes dos mesmos fabricantes.
Nesta página
Proposta da FDA para Mudanças nos Rótulos
Na terça-feira, a Food and Drug Administration anunciou sua intenção de eliminar os rótulos de alerta de suicídio dos medicamentos para emagrecimento GLP-1.
Resultados de Ensaios Abrangentes
A FDA realizou uma análise de 91 ensaios clínicos, comparando receptores de GLP-1 com participantes de placebo. Os pesquisadores descobriram que os 60.338 indivíduos que usaram os medicamentos para emagrecimento não apresentaram maior probabilidade de pensamentos ou ações suicidas do que os 47.572 nos grupos controle.
Medicamentos Alvo da Atualização
Os medicamentos afetados incluem liraglutida, comercializada pela Novo Nordisk como Saxenda; semaglutida, também da Novo Nordisk como Wegovy; e tirzepatida, oferecida pela Eli Lilly como Zepbound, de acordo com a FDA.
Alinhamento com Equivalentes para Diabetes
A nova rotulagem proposta para esses tratamentos de emagrecimento espelhará as informações dos seus equivalentes aprovados para diabetes — especificamente, Ozempic e Rybelsus da Novo Nordisk, junto com Mounjaro da Eli Lilly.
Acompanhamento preciso para a sua rotina
Junte-se a diversas pessoas usando Shotlee para checar e controlar medicações GLP-1 e sintomas sem complicação.
📱 Use o Shotlee Gratuitamente
Junte-se a diversas pessoas usando Shotlee para checar e controlar medicações GLP-1 e sintomas sem complicação.
Esses medicamentos para diabetes nunca apresentaram linguagem referente a pensamentos ou comportamentos suicidas em seus rótulos.
Declarações dos Fabricantes
Um representante da Eli Lilly disse à Pharmaceutical Technology que 'agradecemos a consideração cuidadosa da FDA sobre essa importante questão de segurança. A segurança do paciente é a principal prioridade da Lilly, e continuaremos a trabalhar com a FDA nos próximos passos para garantir que informações de segurança apropriadas estejam disponíveis para os prescritores'.
Um porta-voz da Novo Nordisk informou à Pharmaceutical Technology que 'estamos felizes em ver a recomendação da FDA para remover o alerta sobre o risco de ideação e comportamento suicida ... Priorizamos a segurança do paciente e continuaremos a colaborar de perto com a FDA e outras autoridades regulatórias'.
Informação da fonte
Publicado originalmente por Washington Times.Ler artigo original →