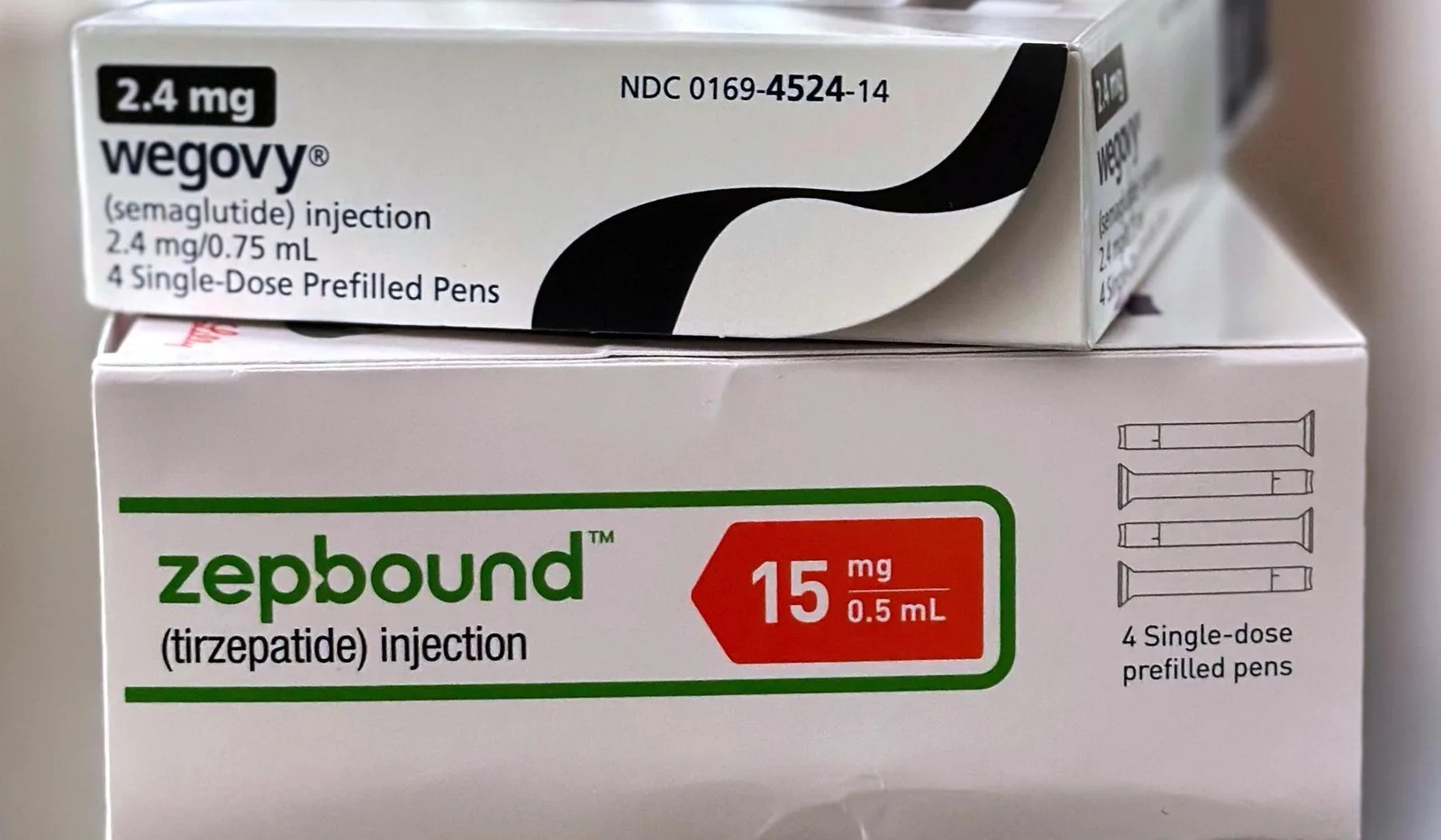
FDA richiede rimozione avvertenza suicidio da farmaci GLP-1 dimagranti
La Food and Drug Administration ha annunciato martedì il desiderio di rimuovere le etichette di avvertimento sul suicidio dai farmaci GLP-1 per la perdita di peso. Una revisione completa di 91 prove cliniche non ha rilevato un rischio maggiore di pensieri o comportamenti suicidari tra gli utenti rispetto ai gruppi placebo. Questo cambiamento allineerà le etichette con quelle degli equivalenti per il diabete degli stessi produttori.
In questa pagina
Proposta FDA per Modifiche alle Etichette
Martedì, la Food and Drug Administration ha annunciato l'intenzione di eliminare le etichette di avvertimento sul suicidio dai farmaci GLP-1 per la perdita di peso.
Risultati dalle Prove Cliniche Complete
La FDA ha condotto un esame di 91 prove cliniche, confrontando i riceventi GLP-1 con i partecipanti al placebo. I ricercatori hanno scoperto che i 60.338 individui che hanno usato i farmaci per la perdita di peso non hanno mostrato una probabilità maggiore di pensieri o azioni suicide rispetto ai 47.572 dei gruppi di controllo.
Farmaci Coinvolti dall'Aggiornamento
I farmaci interessati includono il liraglutide, commercializzato da Novo Nordisk come Saxenda; il semaglutide, anch'esso da Novo Nordisk come Wegovy; e il tirzepatide, offerto da Eli Lilly come Zepbound, secondo la FDA.
Allineamento con i Farmaci per Diabete Equivalenti
La nuova etichettatura proposta per questi trattamenti per la perdita di peso rifletterà le informazioni sui loro equivalenti approvati per il diabete: specificamente, Ozempic e Rybelsus di Novo Nordisk, insieme a Mounjaro di Eli Lilly.
Tracciamento preciso lungo il percorso
Unisciti ai mille che utilizzano Shotlee per tracciare scrupolosamente i farmaci GLP-1 e relativi effetti collaterali.
📱 Usa Shotlee gratuitamente
Unisciti ai mille che utilizzano Shotlee per tracciare scrupolosamente i farmaci GLP-1 e relativi effetti collaterali.
Questi farmaci per il diabete non hanno mai incluso linguaggio relativo a pensieri o comportamenti suicidari nelle loro etichette.
Dichiarazioni dei Produttori
Un rappresentante di Eli Lilly ha dichiarato a Pharmaceutical Technology: 'apprezziamo l'attenta considerazione della FDA su questa importante questione di sicurezza. La sicurezza del paziente è la priorità assoluta di Lilly e continueremo a collaborare con la FDA per i prossimi passi al fine di garantire che le informazioni di sicurezza appropriate siano disponibili ai prescrittori'.
Un portavoce di Novo Nordisk ha riferito a Pharmaceutical Technology: 'siamo lieti di vedere la raccomandazione della FDA di rimuovere l'avvertimento sul rischio di ideazione e comportamento suicidario ... Prioritizziamo la sicurezza del paziente e continueremo a collaborare strettamente con la FDA e altre autorità regolatorie'.
Informazioni sulla fonte
Pubblicato originariamente da Washington Times.Leggi l'articolo originale →