La FDA demande la suppression des avertissements suicide sur les GLP-1 pour perte de poids
La Food and Drug Administration a annoncé mardi son désir de supprimer les avertissements sur le suicide des médicaments GLP-1 pour la perte de poids. Un examen complet de 91 essais a révélé aucun risque accru de pensées ou comportements suicidaires chez les utilisateurs par rapport aux groupes placebo. Ce changement aligne les étiquettes avec celles des équivalents pour diabète des mêmes fabricants.
Sur cette page
Proposition de la FDA pour les changements d'étiquettes
Mardi, la Food and Drug Administration a annoncé son intention d'éliminer les avertissements sur le suicide des médicaments GLP-1 pour la perte de poids.
Résultats des essais cliniques complets
La FDA a examiné 91 essais cliniques, opposant les receveurs de GLP-1 aux participants sous placebo. Les chercheurs ont découvert que les 60 338 personnes ayant utilisé les médicaments pour la perte de poids ne présentaient pas un risque plus élevé de pensées ou d'actions suicidaires que les 47 572 personnes des groupes témoins.
Médicaments concernés par la mise à jour
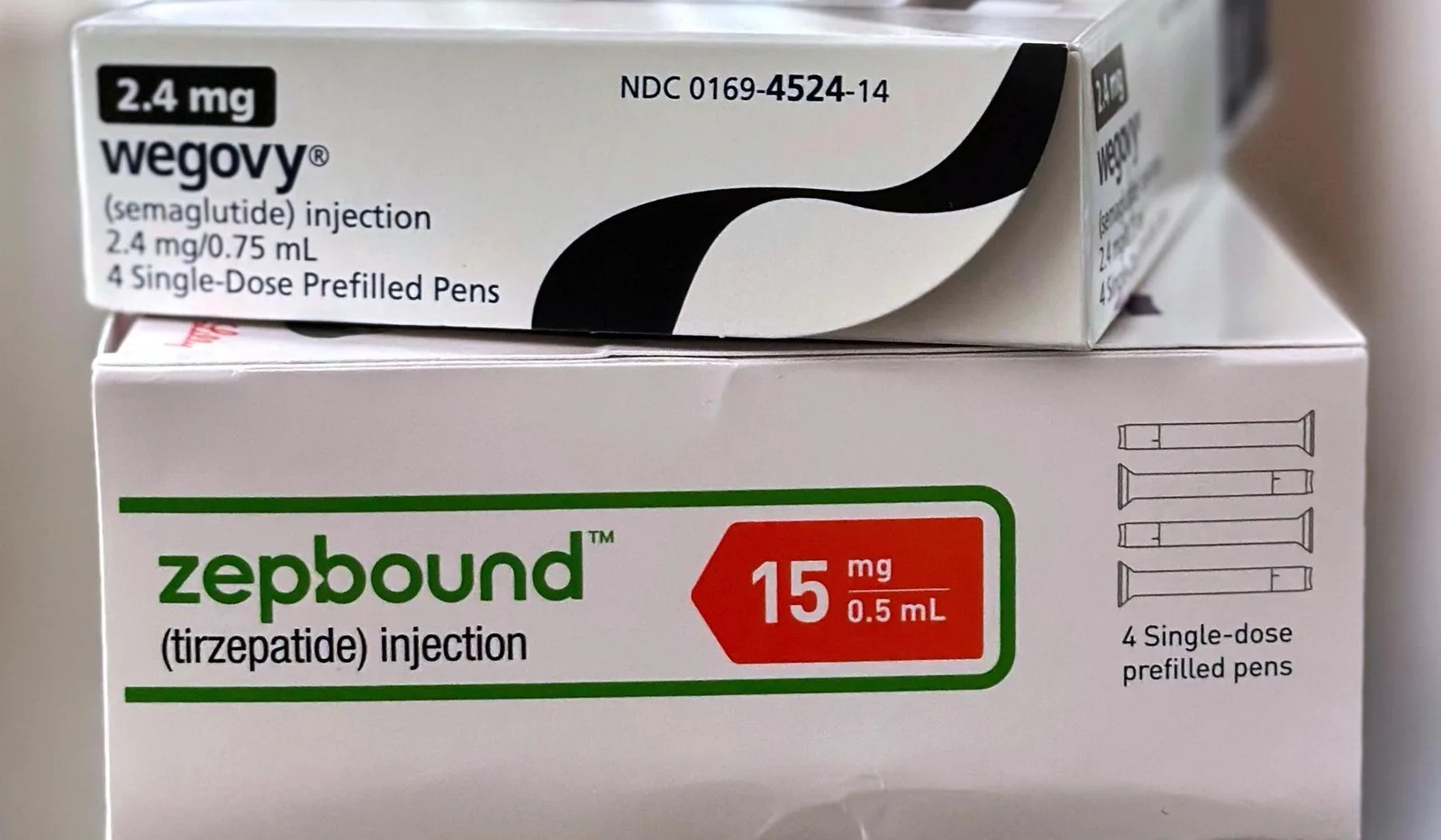
Les médicaments impactés incluent le liraglutide, commercialisé par Novo Nordisk sous le nom de Saxenda ; le sémaglutide, également de Novo Nordisk sous Wegovy ; et le tirzépatide, proposé par Eli Lilly sous Zepbound, selon la FDA.
Alignement avec les équivalents pour diabète
La nouvelle étiquette proposée pour ces traitements contre l'obésité reflétera les informations de leurs homologues approuvés pour le diabète – notamment Ozempic et Rybelsus de Novo Nordisk, ainsi que Mounjaro d'Eli Lilly.
Un suivi précis pour votre santé
Rejoignez les milliers de personnes qui utilisent Shotlee pour suivre avec précision les médicaments GLP-1 et leurs effets de bord.
📱 Utiliser Shotlee gratuitement
Rejoignez les milliers de personnes qui utilisent Shotlee pour suivre avec précision les médicaments GLP-1 et leurs effets de bord.
Ces médicaments pour diabète n'ont jamais comporté de mentions relatives aux pensées ou comportements suicidaires dans leurs étiquettes.
Déclarations des fabricants
Un porte-parole d'Eli Lilly a déclaré à Pharmaceutical Technology : « Nous apprécions la considération minutieuse de la FDA sur cette importante question de sécurité. La sécurité des patients est la priorité absolue de Lilly, et nous continuerons à travailler avec la FDA sur les prochaines étapes pour garantir que les informations de sécurité appropriées soient disponibles pour les prescripteurs. »
Un porte-parole de Novo Nordisk a indiqué à Pharmaceutical Technology : « Nous sommes ravis de voir la recommandation de la FDA de supprimer l'avertissement concernant le risque d'idées et de comportements suicidaires... Nous priorisons la sécurité des patients et continuerons à collaborer étroitement avec la FDA et les autres autorités réglementaires. »
Informations de source
Article publié à l'origine par Washington Times.Lire l'article original →