FDA fordert Entfernung von Suizid-Warnhinweisen bei GLP-1-Abnehmmedikamenten
Die Food and Drug Administration hat am Dienstag ihren Wunsch angekündigt, Suizid-Warnhinweise von GLP-1-Abnehmmedikamenten zu entfernen. Eine umfassende Überprüfung von 91 Studien ergab kein erhöhtes Risiko für suizidale Gedanken oder Verhaltensweisen bei Anwendern im Vergleich zu Placebogruppen. Diese Änderung bringt die Kennzeichnungen mit denen der Diabetes-Äquivalente der gleichen Hersteller in Einklang.
Auf dieser Seite
Vorschlag der FDA für Kennzeichnungsänderungen
Am Dienstag kündigte die Food and Drug Administration ihre Absicht an, Suizid-Warnhinweise von GLP-1-Abnehmmedikamenten zu streichen.
Ergebnisse aus umfassenden Studien
Die FDA hat eine Untersuchung von 91 Studien durchgeführt, in denen GLP-1-Anwender gegen Placebogruppen abgeglichen wurden. Forscher stellten fest, dass die 60.338 Personen, die die Abnehmmedikamenten einnahmen, keine höhere Wahrscheinlichkeit für suizidale Gedanken oder Handlungen aufwiesen als die 47.572 in den Kontrollgruppen.
Betroffene Medikamente durch das Update
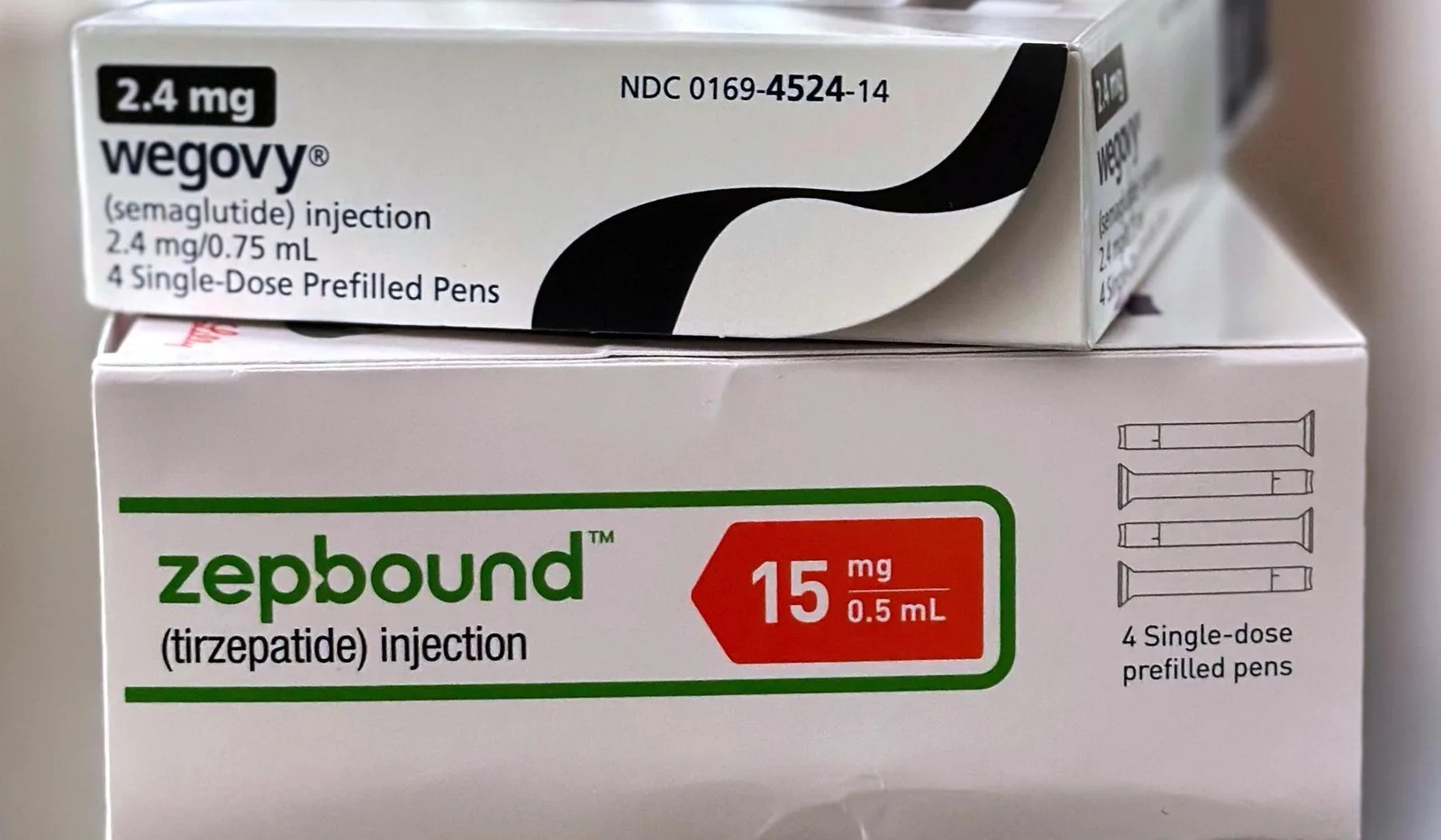
Die betroffenen Medikamente umfassen Liraglutid, vermarktet von Novo Nordisk unter Saxenda; Semaglutid, ebenfalls von Novo Nordisk als Wegovy; und Tirzepatid, angeboten von Eli Lilly unter Zepbound, so die FDA.
Angleichung an Diabetes-Pendants
Die vorgeschlagene neue Kennzeichnung für diese Abnehmbehandlungen wird den Informationen auf ihren für Diabetes zugelassenen Pendants entsprechen – speziell Novo Nordisks Ozempic und Rybelsus sowie Eli Lillys Mounjaro.
Präzises Tracking auf Deinem Weg
Begleite Tausende Nutzer, die mit Shotlee ihre GLP-1-Medikamente und Nebenwirkungen exakt tracken.
📱 Shotlee kostenlos nutzen
Begleite Tausende Nutzer, die mit Shotlee ihre GLP-1-Medikamente und Nebenwirkungen exakt tracken.
Diese Diabetes-Medikamente haben in ihren Kennzeichnungen nie Formulierungen zu suizidalen Gedanken oder Verhaltensweisen enthalten.
Aussagen der Hersteller
Ein Vertreter von Eli Lilly erklärte gegenüber Pharmaceutical Technology: „Wir schätzen die sorgfältige Prüfung der FDA zu diesem wichtigen Sicherheitsaspekt. Die Patientensicherheit ist die oberste Priorität von Lilly, und wir werden weiterhin mit der FDA zusammenarbeiten, um die nächsten Schritte zu gehen und sicherzustellen, dass geeignete Sicherheitsinformationen für Verordner verfügbar sind.“
Ein Sprecher von Novo Nordisk teilte Pharmaceutical Technology mit: „Wir freuen uns über die Empfehlung der FDA, die Warnung bezüglich des Risikos suizidaler Gedanken und Verhaltensweisen zu entfernen ... Wir legen großen Wert auf die Patientensicherheit und werden eng mit der FDA und anderen Regulierungsbehörden zusammenarbeiten.“
Quellenangabe
Ursprünglich veröffentlicht von Washington Times.Originalartikel lesen →