Akuter Schlafmangel verzögert GLP-1-Spitzenreaktion auf Frühstück bei gesunden Männern
Neue Forschung zeigt, dass eine Nacht totaler Schlafmangel die GLP-1-Spitzenreaktion auf das Frühstück bei gesunden jungen Männern signifikant verzögert. Diese Erkenntnis hebt hervor, wie Schlafmangel Schlüssel-Incretinhormone stört, die für Glukoseregulation und Appetitkontrolle wichtig sind. Entdecken Sie das Studiendesign und die Bedeutung für die metabolische Gesundheit.
Auf dieser Seite
- Das Zusammenspiel von Schlafmangel und GLP-1-Reaktion verstehen
- Hintergrund: Schlafmangel und metabolische Störungen
- Studiendesign und Methodik
- Schlüsselergebnisse: Verzögerte GLP-1-Spitze nach Frühstück
- Auswirkungen auf metabolische Gesundheit und GLP-1-Therapien
- Schlüsseleinsichten und handlungsrelevante Tipps
- Schlussfolgerung
- Warum das für die GLP-1-Signalisierung wichtig ist
- Kontrollierte Bedingungen für robuste Ergebnisse
- Vergleiche mit früherer Forschung
- Sicherheitsaspekte und Patientenberatung
Das Zusammenspiel von Schlafmangel und GLP-1-Reaktion verstehen
Akuter Schlafmangel hat sich als entscheidender Faktor für die metabolische Gesundheit herausgestellt, insbesondere durch seine Auswirkungen auf Glucagon-like Peptide 1 (GLP-1), ein zentrales Incretinhormon. Eine Studie in Nutrition & Diabetes mit dem Titel „Akuter Schlafmangel verzögert die GLP-1-Spitzenreaktion auf das Frühstück bei gesunden Männern“ zeigt, wie totaler Schlafmangel (TSD) den normalen postprandialen GLP-1-Anstieg stört. Diese Forschung ist besonders relevant für Interessierte an GLP-1-Medikamenten, Peptidtherapie und Strategien zur Optimierung der Stoffwechselfunktion, da sie Einblicke in die endogenen GLP-1-Dynamiken unter Schlafmangelstress gibt.
GLP-1 spielt eine entscheidende Rolle bei der Verstärkung der Insulinsekretion nach Nährstoffaufnahme, der Unterdrückung von Glukagon, der Verlangsamung der Magenentleerung und der Reduktion der Nahrungsaufnahme. Störungen seiner Sekretion, wie sie durch Schlafmangel induziert werden, könnten zu den erhöhten Risiken für Adipositas und Typ-2-Diabetes beitragen, die in epidemiologischen Daten beobachtet werden. Frühere Studien haben gezeigt, dass akuter Schlafmangel die Nahrungsaufnahme steigert und die Glukosetoleranz sowie die Insulinsensitivität beeinträchtigt, was die Forscher dazu anregte, die Beteiligung von GLP-1 zu untersuchen.
Hintergrund: Schlafmangel und metabolische Störungen
Epidemiologische Beobachtungen verbinden konsequent kurze Schlafdauern mit erhöhten Risiken für Adipositas und Typ-2-Diabetes. Experimentelle Evidenz unterstützt dies: Akuter Schlafmangel erhöht die Nahrungsaufnahme und verschlechtert die Glukosetoleranz und Insulinsensitivität. Als Incretin wird GLP-1 postprandial sezerniert, um die Insulinfreisetzung zu verstärken und den Appetit zu zügeln.
Vorherige Forschung liefert gemischte Erkenntnisse. Eine Studie fand reduzierte GLP-1-Plasmaspiegel am Nachmittag nach fragmentiertem Schlaf bei gesunden Männern, obwohl die 24-Stunden-Werte unverändert blieben – möglicherweise aufgrund der milden Intervention, die REM in Stadium-2-Schlaf verschob. Eine andere berichtete von verringertem GLP-1 bei Frauen (nicht bei Männern) nach drei Nächten mit 4-Stunden-Schlafeinschränkung. Diese Inkonsistenzen unterstreichen die Notwendigkeit kontrollierter Untersuchungen zum Einfluss akuten Schlafmangels auf GLP-1-Profile, was den Rahmen für die aktuelle Untersuchung von 24-Stunden-Serum-GLP-1 bei gesunden jungen Männern unter normalem Schlaf im Vergleich zu TSD schafft.
Warum das für die GLP-1-Signalisierung wichtig ist
Die doppelte Rolle von GLP-1 bei der glykämischen Kontrolle und Sättigung macht es zu einem Eckpfeiler der metabolischen Gesundheit. In der klinischen Praxis imitieren GLP-1-Rezeptoragonisten wie Semaglutid (Ozempic, Wegovy) diese Effekte bei Diabetes und Gewichtsmanagement. Das Verständnis, wie Schlafmangel natürliche GLP-1-Reaktionen dämpft, könnte Patientenberatungen zu Lebensstilfaktoren verbessern, die die Therapieeffizienz steigern, wie z. B. die Priorisierung von Schlaftygiene neben Peptidtherapie.
Studiendesign und Methodik
Die Studie umfasste zwölf gesunde Männer (Mittelwert ± s.e.m., Alter = 21,9 ± 0,7 Jahre; BMI = 24,1 ± 0,6 kg/m²) mit regulären Schlaf-Wach-Rhythmen in den vorherigen 6 Wochen und ohne Medikamente. Akute Erkrankungen wurden durch körperliche Untersuchungen und Labortests ausgeschlossen. Die Teilnehmer gaben schriftliche informierte Einwilligung gemäß der Deklaration von Helsinki und lokaler Ethikgenehmigung. Die Daten stammen aus einer größeren Studie zu den Auswirkungen von Schlafmangel auf den Energieverbrauch, wobei zwei Probanden aufgrund technischer Probleme ausgeschlossen wurden.
Jeder Teilnehmer absolvierte zwei 24-Stunden-Laborsitzungen – Schlaf und TSD – getrennt durch 4 Wochen, nach einer Anpassungsnacht. Ab 18:00 Uhr ruhten die Probanden liegend im Bett bis 13:00 Uhr des nächsten Tages, dann sitzend. In der Schlafbedingung überwachte Polysomnographie (Nihon Kohden GmbH) den Schlaf von 23:00 bis 07:00 Uhr, bewertet nach Standardkriterien. TSD hielt die Probanden unter ~300 Lux Licht wach, mit nicht-erregenden Aktivitäten wie Filmen, Spielen oder Lesen unter Aufsicht.
Körperliche Aktivität und Aufnahme waren standardisiert. Mahlzeiten umfassten: 19:30 Uhr (~1,7 MJ; Kohlenhydrate 0,7 MJ, Fett 0,5 MJ, Protein 0,5 MJ); 08:30 Uhr Frühstück (~3,8 MJ; Kohlenhydrate 1,9 MJ, Fett 1,3 MJ, Protein 0,6 MJ) – speziell 600 ml Fresubin Energy Drink (112,8 g Kohlenhydrate) bei 20 ml/min; und 13:30 Uhr (~4,5 MJ; Kohlenhydrate 1,9 MJ, Fett 1,9 MJ, Protein 0,7 MJ). Am Sitzungsende folgte ein 16,5 MJ ad-libitum-Buffet. Wasser unbegrenzt; keine zusätzliche Nahrung erlaubt.
Blut wurde alle 1,5–3 Stunden in EDTA-Röhrchen entnommen, einschließlich über lange dünne Schläuche während des Schlafs, um Störungen zu vermeiden. Proben zentrifugiert (2000 g, 10 min) und bei -80 °C gelagert. Gesamt-GLP-1 gemessen mittels Millipore-Radioimmunoassay (niedrigste nachweisbare Konzentration 3 pmol/l mit 300 μl Extrakt; Inter-Assay-CV 23 %, Intra-Assay-CV 22 %). Daten normalisiert auf 24-Stunden-Individuenmittelwerte; analysiert mit wiederholten ANOVA (Faktoren Schlaf/TSD und Zeit), post-hoc t-Tests/Wilcoxon und trapezförmiger AUC. Signifikanz bei P < 0,05.
Präzises Tracking auf Deinem Weg
Begleite Tausende Nutzer, die mit Shotlee ihre GLP-1-Medikamente und Nebenwirkungen exakt tracken.
📱 Shotlee kostenlos nutzen
Begleite Tausende Nutzer, die mit Shotlee ihre GLP-1-Medikamente und Nebenwirkungen exakt tracken.
Kontrollierte Bedingungen für robuste Ergebnisse
Dieses rigorose Setup isoliert den Einfluss von Schlaf und kontrolliert Störfaktoren wie Aktivität, Licht und Ernährung – entscheidend für die Reproduzierbarkeit in der metabolischen Forschung.
Schlüsselergebnisse: Verzögerte GLP-1-Spitze nach Frühstück
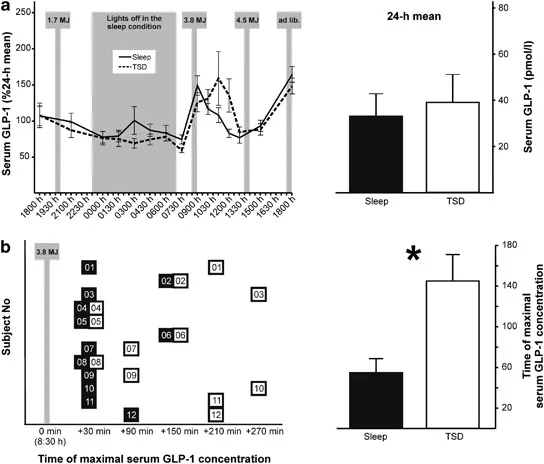
Die Kernbotschaft der Studie entspricht ihrem Titel: Akuter Schlafmangel verzögert die GLP-1-Spitzenreaktion auf das Frühstück bei gesunden Männern. Unter TSD war der postprandiale GLP-1-Anstieg – normalerweise prompt nach der kohlenhydratreichen Mahlzeit um 08:30 Uhr – im Vergleich zum normalen Schlaf verschoben. Während die vollständigen 24-Stunden-Profile nuancierte Unterschiede zeigten, hebt diese spezifische Verzögerung die Rolle von Schlaf bei der zeitlichen Steuerung der Incretinsecretion hervor.
Normalisierte GLP-1-Konzentrationen zeigten Interaktionen Bedingung-×-Zeit, wobei post-hoc-Analysen die Verschiebung der Frühstücksspitze bestätigten. Diese zeitliche Fehlanpassung könnte den metabolischen Schaden durch Schlafmangel untermauern, da zeitgerechtes GLP-1 für die Insulinpotenzierung und Sättigungssignalisierung essenziell ist.
Auswirkungen auf metabolische Gesundheit und GLP-1-Therapien
Diese Ergebnisse erweitern die Evidenz, dass Schlafeinschränkung Incretin-Wege stört und potenziell Adipositas- und Diabetesrisiken verschärft. Eine verzögerte GLP-1-Spitze könnte postprandiale Hyperglykämie verlängern und Hunger steigern, was mit beobachteten Aufnahmezunahmen nach Schlafmangel übereinstimmt.
Für Patienten mit GLP-1-Agonisten unterstreicht dies die Synergie mit Schlaf. Schlechter Schlaf könnte die endogene GLP-1-Unterstützung dämpfen und die Gesamteffizienz mindern. Kliniker könnten 7–9 Stunden nächtlichen Schlaf empfehlen, um Ergebnisse bei Typ-2-Diabetes oder Abnehmprotokollen zu optimieren.
Vergleiche mit früherer Forschung
Im Gegensatz zu fragmentierten-Schlaf-Studien mit nur nachmittäglichen Abfällen erzeugte TSD eine klarere postprandiale Verzögerung. Geschlechtsunterschiede in Einschränkungsstudien (Frauen stärker betroffen) erfordern weitere Vergleiche Mann-Frau.
Sicherheitsaspekte und Patientenberatung
Obwohl TSD extrem ist, ahmt chronisch kurzer Schlaf Risiken nach. Patienten sollten Schlaf mit Anbietern besprechen, besonders bei GLP-1-Medikamenten. Tools wie Shotlee können Schlafmuster, Symptome und Medikamentenreaktionen tracken für personalisierte Anpassungen. Häufige Nebenwirkungen von GLP-1-Therapien (Übelkeit, GI-Probleme) können durch Müdigkeit verschlimmert werden; engmaschig überwachen.
Wer profitiert? Personen mit metabolischen Bedenken – Prädiabetes, Adipositas – könnten Schlaf priorisieren, um natürliches GLP-1 zu stärken. Vor Änderungen Arzt konsultieren, besonders bei Komorbiditäten.
Schlüsseleinsichten und handlungsrelevante Tipps
- Akuter totaler Schlafmangel verzögert die GLP-1-Spitzenreaktion auf Frühstück bei gesunden jungen Männern, gemäß Nutrition & Diabetes-Studie.
- 12 Teilnehmer (Alter ~22, BMI ~24); kontrollierte 24-Stunden-Sitzungen mit standardisierten Mahlzeiten.
- Frühstück: 600 ml, 112,8 g Kohlenhydrate; GLP-1 per Radioimmunoassay analysiert.
- Auswirkungen: Bestärkt Schlafs Rolle bei Incretin-Funktion, relevant für Diabetesprävention und GLP-1-Therapieoptimierung.
- Praktischer Tipp: Konsistent 7–9 Stunden Schlaf anstreben; mit Apps für metabolische Gesundheit tracken.
Schlussfolgerung
Diese Studie beleuchtet, wie bereits eine schlaflose Nacht die GLP-1-Reaktion auf Frühstück stört, mit weitreichenden Folgen für metabolische Signalisierung. Durch Erhalt endogener Rhythmen können Individuen GLP-1-Wege natürlich unterstützen und Peptidtherapien ergänzen. Zukünftige Forschung sollte chronische Effekte, Frauen und Interventionen untersuchen. Vorerst Schlaf priorisieren, um Incretin-Gesundheit zu schützen und kardiometabolische Risiken zu mindern.
Quellenangabe
Ursprünglich veröffentlicht von Nature.Originalartikel lesen →